- Борная кислота
- Лекарственная форма:
- Состав на 100 мл:
- Описание:
- Фармакотерапевтическая группа
- Фармакологическое действие
- Фармакокинетика
- Показания к применению
- Противопоказания
- Способ применения и дозы
- Побочные эффекты
- Передозировка
- Особые указания
- Форма выпуска
- Условия хранения
- Срок годности
- Борная кислота
- Содержание
- Нахождение в природе
- Получение
- Свойства
- Борная кислота в медицине
- Технология спиртовых растворов в условиях аптек
Борная кислота
Лекарственная форма:
раствор для местного применения спиртовой
Состав на 100 мл:
активное вещество: борная кислота 3 г
вспомогательное вещество: этанол (этиловый спирт) 70 % до 100 мл
Описание:
бесцветная прозрачная жидкость с запахом спирта.
Фармакотерапевтическая группа
Фармакологическое действие
Антисептическое средство; коагулирует белки (в т.ч. ферментные) микробной клетки, нарушает проницаемость клеточной оболочки.
Фармакокинетика
Хорошо проникает через кожу и слизистые оболочки; медленно выводится и может накапливаться в органах и тканях. Выводится почками – 50% (в течение 12 ч), остальное количество – в течение 5-7 дней.
Показания к применению
Отит (острый наружный и хронический) без повреждения барабанной перепонки.
Противопоказания
Гиперчувствительность, хроническая почечная недостаточность, перфорация барабанной перепонки; беременность, детский возраст, период лактации.
Способ применения и дозы
Местно. При остром и хроническом отите по 3-5 кап. наносят на турунду и вводят в наружный слуховой проход 2-3 раза в день. Курс лечения не должен превышать 3-5 дней.
Побочные эффекты
Местные реакции: зуд, жжение, гиперемия кожи наружного слухового прохода.
Передозировка
Симптомы острой интоксикации (при случайном приеме внутрь): тошнота, рвота, диарея, гастралгия, нарушение функций сердечно-сосудистой системы, стимуляция или угнетение центральной нервной системы, гиперпирексия, эритематозные высыпания с последующей десквамацией (возможен летальный исход в течение 5-7 дней), нарушение функции почек и печени (в т.ч. желтуха), циркуляторный коллапс, шок, в т.ч. с летальным исходом.
Лечение: симптоматическое. Переливание крови, гемо- и перитонеальный диализ.
Особые указания
Избегать попадания на слизистые оболочки.
Форма выпуска
Раствор для местного применения спиртовой 3%.
По 10, 25, 40 мл во флаконы оранжевого стекла с винтовой горловиной или по 10, 15, 25 мл во флаконы-капельницы, укупоренные пробками полиэтиленовыми и навинчиваемыми крышками.
Каждый флакон с инструкцией по применению помещают в пачку из картона.
Допускается упаковка флаконов без пачки вместе с равным количеством инструкций по медицинскому применению в групповую упаковку.
Условия хранения
В защищенном от света месте при температуре от 15 до 25 o C.
Хранить в недоступном для детей месте.
Срок годности
Не использовать после истечения срока годности.
Источник
Борная кислота
| Борная кислота | |
 | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Ортоборная кислота |
| Хим. формула | H3BO3 |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | 61,83 г/моль |
| Плотность | 1,435 (15 °C) |
| Термические свойства | |
| Т. плав. | 170.9 °C, 444 K, 340 °F |
| Т. кип. | 300 °C, 573 K, 572 °F °C |
| Химические свойства | |
| pKa | 9,24 (I), 12,74 (II), 13,80 (III) |
| Растворимость в воде | |
| Классификация | |
| Рег. номер CAS | 10043-35-3 |
| PubChem | 7628 |
| Рег. номер EINECS | 233-139-2 |
| SMILES | |
| Кодекс Алиментариус | E284 |
| RTECS | ED4550000 |
| ChEBI | 33118 |
| ChemSpider | 7346 |
| Безопасность | |
| Токсичность | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
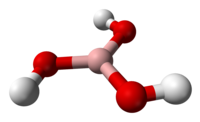
Бо́рная кислота́ (ортоборная кислота или лат. acidum Boricum ) — слабая, одноосновная кислота Льюиса, часто используемая в качестве инсектицида, антисептика, огнезащитного состава, поглотителя нейтронов или предшественника для получения иных химических составов. Имеет химическую формулу H3BO3 (или B(OH)3).
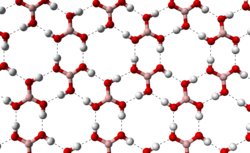
Бесцветное кристаллическое вещество в виде чешуек без запаха, имеет слоистую триклинную решётку, в которой молекулы кислоты соединены водородными связями в плоские слои, слои соединены между собой межмолекулярными связями, длина которых составляет 272пм. Расстояние между соседними слоями — 318пм.
Метаборная кислота (HBO2) также представляет собой бесцветные кристаллы. Она существует в трёх модификациях — наиболее устойчивой γ-НВО2 с кубической решёткой, β-НВО2 с моноклинной решёткой и α-НВО2 с ромбической решёткой.
При нагревании ортоборная кислота теряет воду и сначала переходит в метаборную кислоту, затем в тетраборную H2B4O7. При дальнейшем нагревании обезвоживается до борного ангидрида.
Водные растворы борной кислоты являются смесью полиборных кислот общей формулы Н3m-2nВmО3m-n. В природе встречается в виде минерала сассолина.
Содержание
Нахождение в природе
В природе свободная борная кислота встречается в виде минерала сассолина, в горячих источниках и минеральных водах.
Получение
Борная кислота может быть получена путём смешения буры (Тетрабората натрия) с минеральной кислотой, например, соляной:
N a 2 B 4 O 7 ⋅ 10 H 2 O + 2 H C l → 4 H 3 B O 3 + 2 N a C l + 5 H 2 O <\displaystyle <\mathsf
Также является продуктом гидролиза диборана или тригалогенидов бора [1] :
B 2 H 6 + 6 H 2 O → 2 H 3 B O 3 + 6 H 2 <\displaystyle <\mathsf 
Свойства
Борная кислота проявляет очень слабые кислотные свойства. Она сравнительно мало растворима в воде. Её кислотные свойства обусловлены не отщеплением протона Н + , а присоединением гидроксильного аниона:
B ( O H ) 3 + H 2 O → H [ B ( O H ) 4 ] <\displaystyle <\mathsf 
Она легко вытесняется из растворов своих солей большинством других кислот. Соли её, называемые боратами, производятся обычно от различных полиборных кислот, чаще всего — тетраборной Н2В4О7, которая является значительно более сильной кислотой, чем ортоборная.
Очень слабые признаки амфотерности B(OH)3 проявляет, образуя малоустойчивый гидросульфат бора В(HSO4)3.
При нейтрализации ортоборной кислоты щелочами в водных растворах не образуются ортобораты, содержащие ион (ВО3) 3− , поскольку ортобораты гидролизуются практически полностью, вследствие слишком малой константы образования [В(ОН)4] − . В растворе образуются тетрабораты, метабораты или соли других полиборных кислот:
2 N a O H + 4 H 3 B O 3 ⟶ N a 2 B 4 O 7 + 7 H 2 O <\displaystyle <\mathsf <2NaOH+4H_<3>BO_<3>\longrightarrow Na_<2>B_<4>O_<7>+7H_<2>O>>> 
Мета- и тетрабораты гидролизуются, но в меньшей степени (реакции, обратные приведённым).
В подкисленных водных растворах боратов устанавливаются следующие равновесия:
3 H [ B ( O H ) 4 ] ⇄ H + + [ B 3 O 3 ( O H ) 4 ] − + 5 H 2 O <\displaystyle <\mathsf <3H[B(OH)_<4>]\rightleftarrows H^<+>+[B_<3>O_<3>(OH)_<4>]^<->+5H_<2>O>>> 
При нагревании борная кислота растворяет оксиды металлов, образуя соли.
Со спиртами в присутствии концентрированной серной кислоты образует эфиры:
H 3 B O 3 + 3 C H 3 O H ⟶ 3 H 2 O + B ( O C H 3 ) 3 <\displaystyle <\mathsf
Образование борнометилового эфира В(ОСН3)3 является качественной реакцией на Н3ВО3 и соли борных кислот, при поджигании борнометиловый эфир горит красивым ярко-зеленым пламенем.
Борная кислота в медицине
Борный спирт (лат. Solutio Acidi borici spirituosa ) — раствор борной кислоты в этиловом спирте (как правило, в 70 % этаноле).
Спиртовые растворы борной кислоты в концентрации 0,5 %, 1 %, 2 %, 3 %, 5 % готовятся на 70 % этиловом спирте и применяются в качестве антисептика и как противозудное средство при обтирании здоровых участков кожи вокруг очагов пиодермии, а также в качестве ушных капель.
Борная кислота может быть опасна только при бесконтрольном приёме внутрь. Опасная концентрация в организме человека (а особенно ребёнка) может возникнуть при регулярном применении. Смертельная доза при отравлении через рот для взрослого человека составляет 15-20 г, для детей — 4-5 г [2] .
Борная кислота применяется в медицине с 60-х годов XIX века как антисептическое средство, не раздражающее ран и не имеющее вкуса, запаха и цвета. В современной медицине противомикробная эффективность борной кислоты считается низкой.
Использование борной кислоты в качестве антисептического средства для детей, а также беременных и кормящих женщин было запрещено 2 февраля 1987 года Министерством здравоохранения СССР по рекомендации Фармакологического комитета с формулировкой: «…запретить использование борной кислоты в качестве антисептического средства у детей грудного возраста, а также у женщин в период беременности и лактации в связи с её низкой активностью и высокой токсичностью» [3] .
Источник
Технология спиртовых растворов в условиях аптек
1. Изготовление спиртовых растворов лекарственных веществ
Изготовление спиртовых растворов лекарственных веществ в условиях аптек регламентируется приказом МЗ РФ № 308 от 21.10.97 «Об утверждении инструкции по изготовлению в аптеках жидких лекарственных форм». Водно-спиртовые растворы твердых лекарственных веществ изготавливают в массо-объемной концентрации. Выписанное в рецепте количество спирта соответствует объемным единицам измерения. Норма отпуска спирта учетной концентрации в пересчете на массу составляет 50 г, а в случае указания в рецепте «По специальному назначению» — не более 100 г. Для учета спирта по массе спирта поступающей концентрации используют таблицы, приведенные в Приложении 12 к приказу МЗ РФ № 308 от 21.10.97. Спиртовые растворы готовят непосредственно во флаконе для отпуска. В первую очередь через сухую воронку во флакон всыпают отвешенные порошкообразные лекарственные вещества. Затем через ту же воронку вливают отмеренный цилиндром этиловый спирт. Спиртовые растворы не фильтруют. В случае необходимости (обнаружении в растворе механических включений) спиртовые растворы процеживают через ватный или марлевый тампон. При изготовлении лекарственных форм спирт дозируют по объему, не уменьшая объем, указанный в рецепте, на величину его прироста при растворении лекарственных веществ. Общий объем учитывают при контроле качества лекарственной формы. Изменение объема при растворении лекарственных веществ, учитываемое при контроле, рассчитывают, используя значения коэффициентов увеличения объема (КУО) лекарственных веществ в спиртовых растворах (Приложение 9 к приказу МЗ РФ № 308 от 21.10.97). При изготовлении стандартных спиртовых растворов используют спирт в концентрации, указанной в нормативной документации (Приложение 3 к приказу МЗ РФ № 308 от 21.10.97). Если в прописи рецепта без указания концентрации выписан раствор, представленный в нормативной документации несколькими концентрациями лекарственного вещества, отпускают раствор с меньшей концентрацией, т.е. растворы: — бриллиантового зеленого 1%, — йода 1%, — кислоты борной 1%, — кислоты салициловой 1%, — левомицетина 0,25%, — ментола 1%, — резорцина 1%, — камфоры 2%. Пример: Rp.: Mentholi 1,0 Novocaini 3,0 Anaesthesini 2,5 Spiritus aethylici 50,0 В рецепте не указана концентрация спирта. Прописанный состав отличается по количественному содержанию лекарственных веществ от состава стандартного спиртового раствора — меновазина (ментола 2,5 г, новокаина 1 г, анестезина 1 г, спирта этилового 70% до 100 мл) (Приложение 3 к приказу МЗ РФ № 308 от 21.10.97), в связи с чем при изготовлении лекарственной формы используют спирт этиловый 90%. Во флакон для отпуска темного стекла всыпают через воронку отвешенные на ручных весочках лекарственные вещества: 3 г новокаина, 2,5 г анестезина и 1 г ментола, отмеривают мерным цилиндром и вливают через ту же воронку 50 мл спирта 90%-ного. Общий объем раствора с учетом прироста объема при растворении лекарственных веществ равен 55,6 мл. Отклонение в объеме превышает норму допустимого отклонения (±4%), что учитывают при контроле раствора. По памяти записывают взятые ингредиенты и их количества в паспорте письменного контроля. Флакон укупоривают, оформляют этикеткой «Наружное» и предупредительными этикетками «Беречь от детей», «Беречь от огня», «Хранить в прохладном месте». Срок годности приготовленной лекарственной формы – 10 суток (Приказ МЗ РФ №214 от 16.07.1997 г. «О контроле качества лекарственных средств, изготовляемых в аптеках»).
2. Разбавление этанола
На практике, особенно в условиях аптек лечебно-профилактических учреждений, нередко приходится производить разбавление этанола, например, при изготовлении спирта этилового 70° для обработки кожи при инъекциях, 50° для компрессов и т.д.. При смешении водно-спиртовых растворов с водой или водно-спиртовых растворов разной концентрации имеет место явление контракции (сжатия) – уменьшение объема полученного раствора по сравнению с суммой объемов исходных растворов, сопровождающееся повышением температуры. Изменение величины контракции имеет сложную зависимость от содержания спирта и воды и приводится в справочной литературе [1, с.22]. Явление контракции необходимо учитывать при разбавлении спирта этилового водой и приготовлении спиртовых растворов. При проведении расчетов при разбавлении спирта этилового следует использовать формулу:
Х – необходимое количество (по объему или по массе) исходного водно-спиртового раствора Y – требуемое количество (по объему или по массе) водно-спиртового раствора желаемой концентрации b – концентрация спирта (соответственно по объему или по массе) в водно-спиртовом растворе, который необходимо приготовить а – концентрация спирта (соответственно по объему или по массе) в исходном водно-спиртовом растворе При использовании данной формулы следует обратить особое внимание на единицы измерения: если разведение проводится по объему, то концентрация спирта должна быть выражена в % по объему, если по массе, то концентрация спирта должна быть выражена в % по массе. Разведение спирта по объему позволяет проводить технологические операции достаточно быстро, но с малой точностью, т.к. на результат измерений влияет температура и субъективное восприятие края мениска при отмеривании. С достаточной точностью можно приготовить малые количества спиртовых разведений (до 100 мл) при изготовлении жидких лекарственных форм в ассистентской комнате. При этом разбавляемый спирт отмеривают мерным цилиндром и доводят в том же цилиндре водой до требуемого объема, определяя его по нижнему краю мениска. Недопустимо добавлять воду по теоретически рассчитанной разнице в объемах требуемого и исходного количества спирта, т.к. при этом не учитывается явление контракции. Пример: приготовить 100 мл спирта этилового 50° для компрессов из 96,2° спирта. Х = 100 * (50 / 96,2) = 52 мл Мерным цилиндром отмеривают 52 мл 96,2° спирта и доводят в нем водой до 100 мл. Как правило, в аптеках проводится разбавление спирта в значительных количествах. Для достижения точности концентрации дозирование производят по массе. Спирт этиловый отвешивают в старированную подставку (банку) и добавляют рассчитанное по разнице в массе количество воды, которое можно как отвесить, так и отмерить по объему. Для проведения расчетов при дозировании спирта по массе необходимо выразить концентрацию спирта в % по массе. Общепринятым способом указания концентрации спирта в нормативных документах является % по объему. Осуществить перевод концентрации спирта из % по объему в % по массе и наоборот можно с использованием алкоголеметрической таблицы №1 ГФ ХI, в которой, однако, ряд значений концентраций приходится получать путем интерполяции. На практике для нахождения содержания спирта в процентах по массе (Р) по объемному содержанию спирта (q) целесообразнее пользоваться формулой:
Источник