- 429. Natrii citras pro injectionibus
- Цитрат Натрия
- ВТекстуры в 22 ноября, 2016 — 01:35,Теги сферификация, текстуры, цитрат натрия
- Натрия цитрат
- Фармакологическое действие
- Фармакокинетика
- Показания
- Противопоказания
- С осторожностью
- Беременность и грудное вскармливание
- Способ применения и дозы
- Побочные действия
- Меры предосторожности
- Классификация
- Фармакологические группы
- Код МКБ 10
- Категория при беременности по FDA
- Подробнее по теме
- Цитрат натрия
- Показания к применению
- Возможные аналоги (заменители)
- Действующее вещество, группа
- Лекарственная форма
- Противопоказания
- Как применять: дозировка и курс лечения
- Фармакологическое действие
- Побочные действия
- Особые указания
- Взаимодействие
- Вопросы, ответы, отзывы по препарату Цитрат натрия
- Natrii citras pro injectionibus. Натрия цитрат для инъекций
- Natrii oxybutyras. Натрия оксибутират. Ho-ch2-ch2-ch2-cooNa
- Lithii oxybutyras. Ho-ch2-ch2-ch2-cooLi
- Препараты алифатических аминокислот.
429. Natrii citras pro injectionibus
429. Natrii citras pro injectionibus
Натрия цитрат для инъекций
Natrium citricum pro injectionibus
Тринатриевая соль лимонной кислоты
Описание. Бесцветные кристаллы или белый кристаллический порошок без запаха, солоноватого вкуса, выветривается на воздухе.
Растворимость. Растворим в 1,5 ч. воды, практически нерастворим в спирте.
Подлинность. Препарат дает характерные реакции на цитраты и реакцию Б на натрий (стр. 747; 745).
Прозрачность и цветность раствора. 10% раствор препарата должен Сыть прозрачным и бесцветным.
Щелочность. рН этого раствора 7,8-8,3.
Хлориды. 3 г препарата растворяют в 30 мл воды. 10 мл полученного раствора должны выдерживать испытание на хлориды (не более 0,002%. в препарате).
Сульфаты. 10 мл того же раствора должны выдерживать испытание-на сульфаты (не более 0,01% в препарате).
Тяжелые металлы. 5 мл того же раствора, разведенные водой до 10 мл, должны выдерживать испытание на тяжелые металлы (не более 0,001% в препарате).
Железо. Сульфатная зола из 0,6 г препарата должна выдерживать испытание на железо (не более 0,005%) в препарате).
Соли винной кислоты и другие обугливающиеся примеси. 0,5 г препарата помещают в пробирку, прибавляют 10 мл концентрированной серной кислоты и нагревают на кипящей водяной бане в течение 2 минут. Появляющаяся окраска не должна быть интенсивнее окраски эталона.
Примечание. Приготовление эталона. К 10 мл основного раствора I для определения окраски жидкостей прибавляют 0,2 мл разбавленного раствора метиленового синего, приготовленного из 0,1 мл раствора метиленового синего и 10 мл воды.
Соли щавелевой кислоты. 1 г препарата растворяют в смеси 1 мл воды и 3 мл разведенной соляной кислоты, прибавляют 4 мл спирта и 4 капли раствора хлорида кальция. Через 1 час раствор должен оставаться прозрачным.
Кальций. 1 г препарата помещают в платиновый тигель, осторожно обугливают и прокаливают при температуре около 600° (красное каление). Остаток в тигле растворяют в 2 мл разведенной уксусной кислоты, фильтруют через маленький беззольный фильтр в пробирку, промывают тигель и фильтр водой (2 раза по 3-4 мл). Промывные воды присоединяют к основному раствору и доводят водой до 10 мл. Полученный раствор должен выдерживать испытание на кальций (не более 0,03 % в-препарате).
Потеря в весе при высушивании. Около 0,5 г препарата (точная навеска) сушат в сушильном шкафу при 195-200° до постоянного веса. Потеря в весе должна быть не менее 25% и не более 28%.
Примечание. Определение можно проводить также с помощью-инфракрасной лампы или титрованием реактивом К. Фишера.
Мышьяк. 0,5 г препарата не должны давать реакции на мышьяк.
Количественное определение. Около 1 г препарата (точная навеска) растворяют в свежепрокипяченной и охлажденной воде в мерной колбе емкостью 100 мл и доводят объем раствора водой до метки. 10 мл полученного раствора количественно переносят на колонку с катеонитом КУ-1 или КУ-2 в Н-форме (см. статью «Хроматография», стр. 800). Жидкости дают стекать со скоростью 20-25 капель в минуту. Колонку промывают свежепрокипяченной и охлажденной водой (50-70 мл) до нейтральной реакции на метиловый оранжевый. Фильтрат и промывную воду собирают в колбу и титруют 0,05 н. раствором едкого натра (индикатор — фенолфталеин).
1 мл 0,05 н. раствора едкого натра соответствует 0,004301 г C6H5Na307, которого в пересчете на сухое вещество должно быть не менее 99,0% и не более 101,0%.
Хранение. В хорошо укупоренной таре.
Источник
Цитрат Натрия
ВТекстуры в 22 ноября, 2016 — 01:35,Теги сферификация, текстуры, цитрат натрия
Обладая простой химической структурой, цитрат натрия находит применение во многих сферах . Он может выступать в качестве эмульгатора, секвестранта кальция, регулятора кислотности или консерванта. Цитрат натрия долгое время был важным ингредиентом для химических лабораторий, позволяя регулировать кислотность растворов.
В молекулярной гастрономии цитрат используют для регулирования уровня кислотности, а также для уменьшения содержания кальция. Также он используется в качестве эмульгатора, например в рецепте «реконструированного сыра», позволяя получить гладкую и тягучую текстуру.
Цитрат натрия — слабое основание лимонной кислоты. Существует три типа цитрата натрия: мононатрия цитрат, динатрия цитрат и тринатрий. Чаще всего используют тринатрий.
Функции:
Кроме регулирования кислотности, цитрат натрия играет роль секвестранта (изолирующего вещества), позволяя связывать ионы (например, кальция) между собой.
Альгинат натрия, геллановая камедь, пектин и йотта- каррагинан образуют гели только в присутствии ионов кальция. Но эти же ионы препятствуют растворению гидроколлоидов, приводя к образованию комков. Если жидкость, в которой нужно растворить гидроколлоид содержит кальций, то необходимо использовать пассиватор (в нашем случае цитрат натрия) для обеспечения надлежащей гидратации.
Сферификация- лишь одно из многих примеров применения цитрата натрия.
Жидкость сферифицируется, когда гидроколлоид реагирует с кальцием и образует тонкую пленку. Однако время от времени жидкости, используемые для сферификации, уже содержат большое количество ионов кальция. (особенно часто проблема может быть в водопроводной воде). Секвестранты, вроде цитрата натрия, позволяют уменьшить содержание кальция и предотвратить преждевременное гелеобразование. Также они могут увеличить уровень pH (уменьшить кислотность), в случае, если это требуется для протекания прямой сферификации.
Применение:
Цитрат Натрия используется в рецепте Феррана Адриа “сферические равиоли из манго” для регулирования кислотности. Еще одно применение цитрата в современной кулинарии- рецепт сыра от авторов Modernist Cuisine, где с его помощью выдержанным твердым сырам придается текстура плавленного сыра. Рецепт основан на принципе, описанном еще в 1916 году Джеймсом Крафтом, автором «первого в мире сырного слайса.» Цитрат натрия выступает в роли эмульгатора, позволяя сохранить текстуру.
Свойства :
Температура: растворяется в жидкости любой температуры, но чем выше температура, тем сложнее гидратация.
Текстура: цитрат натрия не обладает собственной текстурой, но изменяет внешний вид других продуктов (например, придает « сливочность » сырам)
Внешний вид: Белые гранулы, напоминающие поваренную соль.
Взаимодействие и толерантность:
Кислотность: Добавление цитрата натрия в нейтральную среду немного увеличит pH раствора. Однако его главное свойство- создание растворов, устойчивых к изменению кислотности. Диапазон pH от 3.0 до 6.3.
Взаимодействие с другими ингредиентами: Цитрат натрия- один из главных пассиваторов кальция, что делает его незаменимым при сферификации. Также цитрат используется совместно с другими гидроколлоидами, такими как альгинат натрия или геллановая камедь. Снижая содержание кальция, цитрат позволяет получать гели однородной текстуры.
Использование:
Концентрация: Необходимое количество цитрата натрия зависит от других ингредиентов, поэтому сложно назвать точную цифру. Он обладает кисло- соленым привкусом, поэтому используйте его в умеренном объеме.
Для эмульгирования сыра требуется 4 % цитрата натрия на 100 % сыра. Для приготовления сырных слайсов используйте 3.3 % цитрата, 1.5 % йотта- каррагинана и 0,5 % каппа- каррагинана.
Для использования в качестве пассиватора вам потребуется от 0.07 до 0.4 % в зависимости от жидкости и концентрации гидроколлоида.
Для сферификации, количество цитрата натрия зависит от количества кальция. Наилучшая концентрация- 0.25 % , но при необходимости ее можно увеличить.
Источник
Натрия цитрат
Фармакологическое действие
Натрия цитрат — антикоагулянтное средство. Связывает Ca 2+ (Ⅳ плазменный фактор свёртывания крови) и ингибирует гемокоагуляцию (in vitro). Повышает содержание Na + в организме, повышает щелочные резервы крови. Изменяет реакцию мочи с кислой на щелочную, способствует исчезновению симптомов дизурии.
Фармакокинетика
После абсорбции метаболизируется до бикарбоната, экскретируемого мочой и повышающего её объём и кислотность.
Показания
Консервирование крови, симптоматическое лечение цистита.
Противопоказания
Повышенная чувствительность к натрия цитрату.
С осторожностью
Заболевания сердца, почек, артериальная гипертензия, сахарный диабет, диета с низким содержанием соли, беременность, лактация.
Беременность и грудное вскармливание
При беременности и в период лактации следует применять с особой осторожностью.
Способ применения и дозы
Внутрь 3 раза в сутки в течение 48 часов. Режим дозирования индивидуальный, в зависимости от лекарственной формы.
Побочные действия
Снижение аппетита, тошнота, рвота, боль в животе, повышение артериального давления.
Меры предосторожности
У мужчин и детей цистит часто имеет бактериальную природу, поэтому применение натрия цитрата не рекомендуется. Не следует часто повторять курс лечения. Если по окончании курса лечения симптомы цистита остаются, необходимо верифицировать диагноз.
Классификация
Фармакологические группы
Код МКБ 10
Категория при беременности по FDA
N ( не классифицировано FDA )
Поделиться этой страницей
Подробнее по теме
Ознакомьтесь с дополнительной информацией о действующем веществе Натрия цитрат:
Источник
Цитрат натрия
Показания к применению
Консервирование крови, симптоматическое лечение цистита.
Возможные аналоги (заменители)
Действующее вещество, группа
Лекарственная форма
Противопоказания
Гиперчувствительность к компонентам препарата.
C осторожностью. Заболевания сердца, почек, артериальная гипертензия, сахарный диабет, беременность, период лактации, гипосолевая диета.
Как применять: дозировка и курс лечения
Внутрь, по 1 пакету препарата (предварительно растворив в 1 стакане воды) 3 раза в день, в течение 2 дней.
Фармакологическое действие
Антикоагулянтное средство. Применение препарата снижает свертываемость крови, повышает щелочные резервы крови, защелачивает мочу. Связывает Ca2+ (IV плазменный фактор свертывания крови) и делает невозможной гемокоагуляцию (in vitro). Повышает концентрацию Na+ в организме.
Изменение реакции мочи под воздействием препарата с кислой на щелочную приводит к исчезновению дизурических явлений.
Побочные действия
Аллергические реакции на компоненты препарата.
Снижение аппетита, тошнота, рвота, боль в животе, повышение АД.
Особые указания
Не следует часто повторять курс лечения препаратом. В случае сохранения симптомов цистита необходимо верифицировать диагноз. У мужчин и детей цистит часто имеет бактериальную природу, поэтому не рекомендуется назначать лечение препаратом этим пациентам.
Взаимодействие
Значимого лекарственного взаимодействия при лечении совместно с другими препаратами не выявлено.
Вопросы, ответы, отзывы по препарату Цитрат натрия
Активные компоненты:
Ново-Пассита экстракт жидкий (получаемый из корневищ с корнями валерианы лекарственной, травы мелиссы лекарственной, травы зверобоя продырявленного, листьев и цветков боярышника однопестичного или колючего, травы пассифлоры инкарнатной (страстоцвета), соплодий хмеля обыкновенного, цветков бузины черной) 7,75 г; Гвайфенезин — 4,00 г в 100 мл раствора
Вспомогательные вещества:
натрия цикламат, камедь ксантановая, сахарный сироп инвертный, натрия бензоат, натрия сахарин моногидрат, этанол 96%, аромат апельсиновый, натрия цитрат дигидрат, мальтодекстрин, пропиленгликоль, вода очищенная.
Приведенная информация предназначена для медицинских и фармацевтических специалистов. Наиболее точные сведения о препарате содержатся в инструкции, прилагаемой к упаковке производителем. Никакая информация, размещенная на этой или любой другой странице нашего сайта не может служить заменой личного обращения к специалисту.
Источник
Natrii citras pro injectionibus. Натрия цитрат для инъекций
Описание: белые кристаллы или кристаллический порошок без запаха, выветривающиеся на воздухе
Растворимость: легко – в воде, практически нерастворим в спирте
Получение: взаимодействие лимонной кислоты с карбонатом Nа. Полученную соль перекристаллизовывают из спирта.
Подлинность: ИКС, реакция А на цитраты (с хлоридом кальция):
2 


Осадок растворим в HCl.
1. Реакция Б на цитраты: при нагревании цитрата с уксусным ангидридом через 20-40 секунд развивается карминово-красное окрашивание
2. Реакция Штаре:


Выпадает белый кристаллический осадок.
3. С реактивом Денеже: свежеприготовленный раствор основного сульфата ртути.

Чистота: раствор должен быть прозрачным и бесцветным; рН 7,8-8,3; недопустимы As (III), допустимы общие.
Специфические: тартраты – насыщенный раствор + ацетатный буфер – раствор должен быть прозрачен.
Оксалаты: навеску растворяют в воде, прибавляют HCl, спирт и CaCl2, оставляют на час, раствор должен остаться прозрачным.
Потеря в массе при выслушивании – 25-28%, микробиологическая чистота
Количественное определение: неводное титрование
2. натрия цитрат + 3CH3COOH 3Na + + 3CH3COO — + лимонная кислота
3. CH3COO — + CH3COOH2 + 2CH3COOH
ГФX: ионобменная хроматография
Цитарт натрия + [катионит]Н + [катионит]3Na + + лимонная кислота.
Титруют NaOH с фенолфталеином. f=1/3.
натрия цитрат + 3HCl 
2. Обратная аргентометрия:
натрия цитрат + 3AgNO3 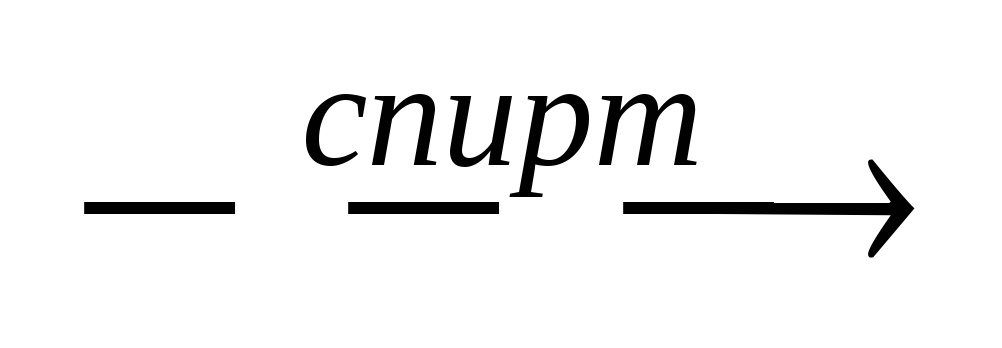
Избыток нитрата серебра оттитровывают роданометрически (NH4SCN) .f=1/3
3. Образование комплекса с медью – прямая куприметрия (CuSO4) с мурексидом.
Хранение: сухое прохладное место
Применение: консервант препаратов крови.
Natrii oxybutyras. Натрия оксибутират. Ho-ch2-ch2-ch2-cooNa
Описание: белый с желтоватым оттенком гигроскопичный порошок. ЛР в воде, Р в спирте, ПНР в эфире, хлороформе.
Получение: из -бутиролактона (специфическая примесь)
Подлинность: ИКС, Б – на Na; лактона – гидроксамовая проба
Количественное определение: неводное титрование f=1; прямая ацидиметрия f=1.
Хранение: список Б, в сухом, защищенном от света месте.
Применение: снотворное, неингаляционный наркоз, порошки, ампулы, сиропы, концентрат (66,7%).
Lithii oxybutyras. Ho-ch2-ch2-ch2-cooLi
Подлинность: окрашивает пламя в фиолетовый цвет, рефрактометрия.
Количественное определение: неводное титрование.
Хранение: список Б
Применение: в психиатрии.
Препараты алифатических аминокислот.
Аминокислоты – соединения природного происхождения, являются строительным материалом для конструкции природных белков и пептидов. Характерная особенность – наличие амино- и карбоксилоной групп. Природные аминокислоты – бесцветные, белые и желтоватого оттенка кристаллические субстанции, хорошо растворимые в воде, хуже в органических растворителях. Некоторые имеют запах.
1. Природные объекты – мясо, молоко, кожа. Получают гидролизом.
2. Синтетические – более 70% всех получаемых аминокислот. Синтезируют на основе галогенкарбоновых кислот или амномалонового эфира.
Тесно связано с физическими свойствами ассиметрического атома углерода (оптическая активность).
1. -COOH, -NH2 придают свойства амфотерности. АК взаимодействуют и с кислотами и со щелочами, способны образовывать комплексы с медью, серой, цинком, свинцом и др.
2. COO — , NH3 + (образование цветтер-иона).
3. Мало и медленно, но растворимы в воде, лучше в горячей, нерастворимы или плохо растворимы в органических растворителях
Источник








