Рецепт соли тяжелых металлов
9. Соли тяжелых металлов
Соли тяжелых металлов оказывают противомикробный эффект, инактивируя ферменты, необходимые для жизнедеятельности микроорганизмов. Инактивация ферментов происходит путем взаимодействия ионов тяжелых металлов с сульфгидрильными группами (SH-группы) ферментов.
На кожу и слизистые оболочки соли тяжелых металлов оказывают выраженное местное действие. В зависимости от ряда условий местное действие этих веществ может быть вяжущим, раздражающим или прижигающим.
Механизм местного действия солей тяжелых металлов обусловлен их способностью реагировать с белками тканей. В результате такого взаимодействия белки свертываются и образуют с ионами металлов альбуминаты (соединения типа белковых солей металлов). При этом, если происходит частичное свертывание белков только в самых поверхностных слоях тканей, наблюдается вяжущий или раздражающий эффект, имеющий обратимый характер. В случае свертывания белков, охватывающего значительную массу тканевых клеток и вызывающего их гибель, возникает прижигающий эффект, при котором происходят необратимые изменения тканей в виде некроза.
По силе противомикробного и местного действия тяжелые металлы могут быть расположены в следующем порядке: Hg, Ag, Fe, Cu, Zn, Bi, Pb, где наиболее активными являются ионы ртути, а наименее активными — ионы свинца.
При применении солей тяжелых металлов для антисептики и дезинфекции необходимо учитывать, что сила их противомикробного действия значительно уменьшается в средах с высоким содержанием белка (например, в присутствии гноя, крови и т. п.), в связи с чем эти вещества непригодны для обеззараживания выделений.
В качестве антисептических средств применяют препараты ртути (ртути дихлорид), серебра (серебра нитрат, протаргол), цинка (цинка сульфат) и висмута (дерматол, ксероформ).
Ртути дихлорид (сулема) оказывает сильное противомикробное и местное раздражающее действие. Применяется для дезинфекции белья, предметов ухода за больными и т. п. Обладает высокой токсичностью для человека. Легко всасываясь через кожу и слизистые оболочки, может вызывать тяжелые отравления. В связи с этим при работе с препаратом следует соблюдать большую осторожность.
Другие соли ртути (ртути оксицианид, ртути окись желтая и т. д.), отличающиеся от ртути дихлорида меньшей токсичностью и менее выраженным раздражающим действием на кожу, применяются в качестве антисептических средств для лечения гнойно-воспалительных поражений кожи и слизистых оболочек при конъюнктивитах, кератитах, блефаритах и т. п.
Серебра нитрат (ляпис) наряду с противомикробными свойствами обладает в малых концентрациях (до 2%) вяжущим, а в больших (5% и более) прижигающим действием. Применяется для лечения кожных язв, эрозий, а также при поражениях слизистых оболочек глаза (трахома, конъюнктивит) и гортани (ларингит). В акушерской практике серебра нитрат применяют для профилактики бленнореи у новорожденных. В качестве прижигающего средства серебра нитрат используют для прижигания избыточных грануляций и бородавок.
Протаргол — недиссоциирующее органическое соединение серебра, обладающее антисептическими, вяжущими и противовоспалительными свойствами. Прижигающего действия на ткани не оказывает. Растворы протаргола применяют для промывания мочевого пузыря и уретры, лечения гнойных конъюнктивитов и бленнореи, а также для смазывания слизистых оболочек верхних дыхательных путей при их воспалительных поражениях.
В качестве заменителя протаргола в практике часто используется колларгол, также являющийся недиссоциирующим соединением серебра. По основным свойствам и применению колларгол соответствует протарголу.
Цинка сульфат как антисептическое и вяжущее средство применяется в виде растворов главным образом при воспалительных поражениях слизистых оболочек глаза (конъюнктивит), гортани (ларингит) и мочеиспускательного канала (уретрит).
Дерматол и ксероформ относятся к органическим соединениям висмута. По сравнению с соединениями других тяжелых металлов они обладают относительно слабыми антисептическими и вяжущими свойствами. Дерматол и ксероформ применяют наружно в виде присыпок и мазей для лечения воспалительных заболеваний кожи и слизистых оболочек. Особенно благоприятный эффект указанные препараты дают при мокнущих поражениях кожи (в частности, при экземе, дерматитах), так как наряду с противомикробным и вяжущим одни оказывают подсушивающее действие, которое объясняется их адсорбирующими свойствами.
Отравления солями тяжелых металлов. Соединения большинства тяжелых металлов, за исключением солей ртути, плохо всасываются через кожу, слизистые оболочки и из желудочно-кишечного тракта. Поэтому с практической точки зрения наибольший интерес представляют отравления соединениями ртути. Особенно высокой токсичностью отличаются легкодиссоциирующие неорганические соли ртути, например ртути дихлорид.
Острые отравления, возникающие после приема препаратов ртути внутрь, характеризуются симптомами, которые обусловлены: а) раздражающим и прижигающим действием соединений ртути на желудочно-кишечный тракт; б) резорбтивным действием ионов ртути; в) действием ртути на путях выделения
Раздражающее и прижигающее действие препаратов ртути на слизистые оболочки желудочно-кишечного тракта развивается вскоре после приема препаратов внутрь. При этом появляются металлический вкус и чувство жжения во рту, боли в животе, тошнота и рвота (нередко с примесью крови), усиление слюноотделения. В первые часы отравления в связи с резким раздражением желудочно-кишечного тракта и возникновением в нем острых болей возможно развитие шока.
Резорбтивное действие ионов ртути развивается уже в первые часы отравления и проявляется признаками токсического влияния ионов ртути на ЦНС (вначале возбуждение ЦНС, судороги, затем ее угнетение), нарушениями деятельности сердечно-сосудистой системы (сердечная слабость, падение артериального давления, слабый и частый пульс) и функции почек (вначале усиление, затем уменьшение мочеотделения).
Действие ионов ртути на путях выделения развивается на 2-3-й сутки от момента приема яда. Ионы ртути выделяются преимущественно слизистыми оболочками пищеварительного тракта и почками, в связи с чем у пострадавших развивается стоматит, язвенный колит и поражение почек.
Помощь при острых отравлениях препаратами ртути сводится к следующему. Вначале предпринимают меры к удалению и предупреждению всасывания яда из желудочно-кишечного тракта. С этой целью пострадавшему дают внутрь молоко, яичный белок (для связывания ртути белком), осторожно промывают желудок водой с активированным углем. Затем назначают внутрь активированный уголь и солевое слабительное (магния сульфат).
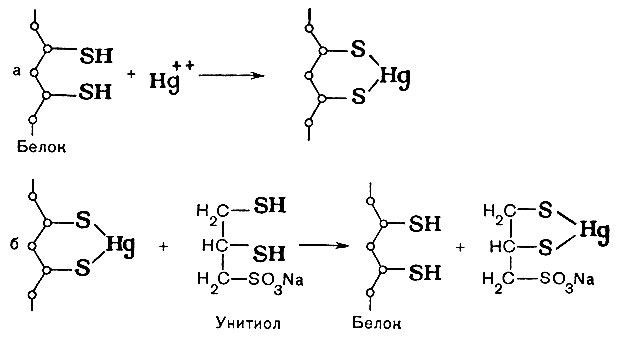
Для предупреждения и купирования резорбтивного действия ионов ртути рекомендуется как можно раньше начать парентеральное введение антидотов. В качестве антидотов при отравлении ртутью используют унитиол и натрия тиосульфат. Принцип действия унитиола заключается в том, что этот антидот, являясь веществом, содержащим SH-группы (сульфгидрильные группы), связывает ионы ртути и тем самым предупреждает блокирование ртутью SH-групп белков и ферментов организма (рис. 28).
Рис. 28. Схема антитоксического действия унитиола при отравлениях солями тяжелых металлов. а — взаимодействие белка (фермента) с ионами ртути; б — защитное действие унитиола
Действие натрия тиосульфата сводится к тому, что ионы ртути образуют с этим веществом неядовитые соли (сульфиты). Натрия тиосульфат при отравлениях препаратами ртути вводят внутривенно в виде 30% раствора по 5-10 мл. Наряду с указанными антидотами рекомендуется внутривенное введение растворов глюкозы.
Кроме того, при терапии отравлений препаратами ртути используют средства симптоматической терапии. Так, при сильных болях и шоке вводят анальгетики (морфин, промедол), при падении артериального давления — сосудосуживающие средства (эфедрин и др.) и т. д.
Отравления солями других тяжелых металлов (серебро, цинк, медь) проявляются теми же симптомами, что и отравления солями ртути. Общие принципы помощи при отравлениях солями цинка и меди в основном аналогичны принципам терапии отравлений соединениями ртути. Так как ионы серебра образуют с ионами хлора плохо растворимые соединения, при отравлениях солями серебра желудок промывают 1-2% раствором натрия хлорида, после чего в качестве слабительного назначают касторовое масло.
Ионы серебра образуют с тиосульфатом натрия растворимые комплексы, в связи с чем тиосульфат натрия нельзя использовать в качестве антидота при отравлении солями серебра, так как в подобных случаях он почти неэффективен.
Ртути дихлорид, Hydrargyri dichloridum — тяжелый белый порошок или белые кристаллы, растворимые в воде и спирте.
Применяют только наружно для дезинфекции в виде 0,1% (1:1000) или 0,2% (1:500) раствора. В связи с высокой токсичностью растворы препарата подкрашивают эозином в розовый цвет, чтобы отличать их от других применяемых растворов, а посуду, содержащую растворы, маркируют этикетками: «Яд», «Только для наружного применения», «Обращаться с осторожностью».
Формы выпуска: порошок; таблетки по 0,5 и 1 г, окрашенные эозином в розовый или красно-розовый цвет. Таблетки предназначены только для наружного Применения (для приготовления растворов).
Хранение: список А.
Серебра нитрат, Argenti nitras — бесцветные, прозрачные кристаллы в виде пластинок или белых кристаллических палочек. Легко растворим в воде. На свету темнеет. С галогенами (хлориды, йодиды, бромиды) выпадает в осадок.
Наружно в качестве антисептического и вяжущего средства применяют в виде 0,25-2% растворов и 1-2% мазей. Как прижигающее средство используют в виде 5-10% растворов или per se в виде ляписных карандашей (Stillius Lapidis). При хронических гастритах и язвенной болезни желудка серебра нитрат иногда назначают внутрь в виде 0,05-0,06% раствора по 1 столовой ложке 3 раза в день как вяжущее и противовоспалительное средство.
Высшие дозы (для взрослых): внутрь — разовая 0,03 г, суточная 0,1 г.
Хранение: список А; в защищенном от света месте.
Протаргол, Protargolum — коричнево-желтый или коричневый порошок без запаха, слабогорького и слегка вяжущего вкуса, легко растворимый в воде.
Применяют в виде растворов: для смазывания слизистых оболочек верхних дыхательных путей (1-5% раствор), промывания мочеиспускательного канала и мочевого пузыря (1-3% раствор) и в глазных каплях (1-3% раствор).
Форма выпуска: порошок.
Хранение: в защищенном от света месте.
Цинка сульфат, Zinci sulfas — бесцветные, прозрачные кристаллы или мелкокристаллический порошок вяжущего вкуса. Легко растворим в воде.
Применяют наружно в виде 0,1-0,5% раствора (глазные капли, спринцевания).
Формы выпуска: порошок; глазные капли (0,25% или 0,5% раствор цинка сульфата и борной кислоты 2%); тюбики-капельницы по 1,5 мл.
Хранение: список Б.
Дерматол, Dermatolum — см. главу 1, 2 (препараты).
Ксероформ, Xeroformium — см. главу 1, 2 (препараты).
Источник
федеральное бюджетное учреждение здравоохранения «Центр гигиены и эпидемиологии в Республике Марий Эл»
Общие факты про тяжелые металлы
Известно более 40 элементов, которые относят к тяжелым металлам. Они имеют атомную массу больше 50 а.е. Как не странно именно эти элементы обладают большой токсичностью даже при малой кумуляции для живых организмов. V, Cr, Mn, Fe, Co, Ni, Cu, Zn, Mo. Pb, Hg, U, Th. все они входят в эту категорию. Даже при их токсичности, многие из них являются важными микроэлементами, кроме кадмия, ртути, свинца и висмута для которых не нашли биологическую роль.
Откуда же поступают тяжелые металлы в нашу среду обитания? Причины присутствия таких элементов могут быть сточные воды с разных промышленных объектов занимающийся черной и цветной металлургией, машиностроением, гальванизацией. Некоторые химические элементы входят в состав пестицидов и удобрений и таким образом могут быть источником загрязнения местных прудов.
Многие тяжелые металлы, такие как железо, медь, цинк, молибден, участвуют в биологических процессах и в определенных количествах являются необходимыми для функционирования растений, животных и человека микроэлементами. С другой стороны, тяжёлые металлы и их соединения могут оказывать вредное воздействие на организм человека, способны накапливаться в тканях, вызывая ряд заболеваний. Не имеющие полезной роли в биологических процессах металлы, такие как свинец и ртуть, определяются как токсичные металлы. Некоторые элементы, такие как ванадий или кадмий, обычно имеющие токсичное влияние на живые организмы, могут быть полезны для некоторых видов.
Ртуть, свинец, кадмий входят в общий перечень наиболее важных загрязняющих веществ окружающей среды, согласованный странами, входящими в ООН.
Кадмий является относительно редким и рассеянным элементом, в природе концентрируется в минералах цинка. Поступает в природные воды в результате смыва почв, выветривания полиметаллических и медных руд, и со сточными водами рудообогатительных, металлургических и химических производств. Кадмий в норме присутствует в организме человека в микроскопических количествах. Загрязнение кадмием может возникнуть во время выщелачивания почв, при разложения разных микроорганизмов которые его накапливают, а также из-за миграции из медных и полиметаллических руд.
Уровень кадмия в чистых реках и озерах колеблется на уровне меньше микрограмма на литр, в загрязнённых водах уровень этого элемента доходит до нескольких микрограммов на литр.
Некоторые исследователи считают, что кадмий, в малых количествах, может быть важным для нормального развития животных и человека. Повышенные концентрации кадмия очень опасных для живых организмов. При накоплении организмом соединений кадмия поражается нервная система, нарушается фосфорно-кальциевый обмен. Хроническое отравление приводит к анемии и разрушению костей. Хроническое отравление кадмием разрушает печень и почки, приводя к сильнейшему нарушению функции почек. Избыток кадмия нарушает метаболизм металлов, нарушает синтез ДНК.
Загрязнены мышьяком в основном районы, которые находятся близко к минеральным рудников с высоким содержанием этого элемента (вольфрамовые, медно-кобальтовые, полиметаллические руды). Очень малое количество мышьяка может произойти при разложении живых организмов. Благодаря водным организмам, он может усваиваться этими. Интенсивное усваивание мышьяка из раствора замечается в период бурного развития планктона.
В реках, как правило, содержание мышьяка очень низкое (на уровне мкг/л), а в морях — в среднем 3 мкг/л. Некоторые минеральные воды могут содержать большие количества мышьяка (до несколько миллиграммов на литр).
Больше всего мышьяка могут, содержат подземные водохранилища — до несколько десяток миллиграммов на литр.
Его соединения очень токсичны для всех животных и для человека. В больших количествах, нарушаются процессы окисления и транспорт кислорода к клеткам.
Мышьяк относится к числу наиболее сильных и опасных ядов. В присутствии кислорода быстро образует очень ядовитый мышьяковистый ангидрид. При пероральном отравлении высокая концентрация мышьяка наблюдается в желудке, кишечнике, печени, почках и поджелудочной железе, при хроническом отравлении постепенно накапливается в коже, волосах и ногтях. Процессе отравления приводит к периферическойнейропатии и параличу конечностей. Мышьяк считается канцерогенным для человека.
Ртуть переносится в океан с материковым стоком (прежде всего — из стока промышленных вод) и через атмосферу. В составе атмосферной пыли содержится около 12 тыс. т. ртути. До трети от этого количества образуется при выветривании пород, содержащих ртуть. Ртуть антропогенного происхождения попадает в атмосферу в первую очередь при сжигании угля на электростанциях. Около половины годового промышленного производства этого металла (910 тыс. тонн) попадает в океан. Некоторые бактерии переводят токсичные хлориды ртутив ещё более токсичную метилртуть. Соединения ртути накапливается многими морскими и пресноводными организмами в концентрациях, во много раз превышающих содержание её в воде.
Употребление в пищу рыбы и морепродуктов неоднократно приводило к ртутному отравлению населения. Так, к 1977 году насчитывалось 2800 жертв болезни Минамата, причиной которой послужило поступление в залив со сточными водами отходов предприятий, на которых в качестве катализатора использовалась хлористая ртуть. Соединения ртути высокотоксичны для человека.
Ртуть поступает в окружающую среду при производстве и использовании ртути в химической и электрохимической промышленности. Металлическая ртуть попадает в комнатный воздух из разбитых градусников и люминесцентных ламп.
Ртуть токсична в любой своей форме. Ртуть в природных условиях довольно быстро превращается в летучее токсическое соединение — хлорид метилртути. В организме ионы метилртути быстро попадают в эритроциты, печень и почки, оседают в мозге, вызывая серьезные необратимые кумулятивные нарушения ЦНС. Это приводит, к конце концов, к общему и церебральному параличу, деформации конечностей, особенно пальцев, затрудненному глотанию, конвульсиям и смерти.
Свинец— рассеянный элемент, содержащийся во всех компонентах окружающей среды: в горных породах, почвах, природных водах, атмосфере, живых организмах. Помимо того, свинец поступает в окружающую среду в результате хозяйственной деятельности человека. До запрета на использование в топливе в качестве антидетонатора тетраэтилсвинца в начале XXI века, выхлопные газы транспорта были заметным источником свинца в атмосфере. С континентальной пылью в атмосфере океан получает 20-30 тысяч тонн свинца в год.
В организм человека свинец попадает как с пищей и водой, так и из воздуха. Свинец может выводиться из организма, однако малая скорость выведения может приводить к накоплению в костях, печени и почках.
Свинец известен как токсическое вещество почти 5 тысяч лет среди греческих и арабских ученыхХроническое отравление свинцом постепенно приводит к нарушениям функций почек, нервной системы, анемии. Токсичность свинца увеличивается при недостатке в организме кальция и железа.
Наиболее восприимчива к свинцу гематопоэтическая система, особенно у детей. Для женщин свинец представляет особую опасность, так как этот элемент обладает способностью проникать через плаценту и накапливаться в грудном молоке. Свинец вызывает обширные патологические изменения в нервной системе, крови, сосудах, активно влияет на синтез белка, энергетический обмен клетки и ее генетический аппарат. Он угнетает окисление жирных кислот, нарушает белковый, липидный и углеводный обмены, способен занимать кальций в костях. Свинец нарушает деятельность сердечно-сосудистой системы, вызывая изменения электрической и механической активности сердечной мышцы. Воздействие свинца нарушает женскую и мужскую репродуктивную систему.
Исследователи изучили процесс накопления свинца в почве. Из атмосферы в почву свинец попадает чаще всего в форме оксидов, где постепенно растворяется, переходя в гидроксиды, карбонаты или форму катионов.
Установлено, что в слое глубиной до 5 см свинец накапливается более интенсивно, чем медь, молибден, железо, никель и хром. И это плохо, поскольку из всего этого ряда свинец – самый ядовитый. Отмечена интересная особенность растений – различных своих частях накоплять различное количество свинца. Например, салат и сельдерей в листьях накапливают значительно больше свинца, чем в корнях, а морковь и одуванчик – наоборот.
Отмечено активное накопление свинца в капусте и корнеплодах, причем именно в тех, которые повсеместно употребляются в пищу; например, отмечают большое содержание свинца в картофеле.
Но рекордсменом среди растений по стойкости к соединениям свинца являются дрожжи. Биологи утверждают, что дрожжи могут поглощать огромные количества свинца в виде уксуснокислой соли – до 15 тысяч частей на миллион частей веса дрожжей – без всякого угнетения обмена веществ. Так может быть дрожжи помогут в борьбе с загрязнением солями свинца? Хлористый и йодистый свинец угнетают брожение. Но — нет, дрожжи – рекордсмен по «свинцовостойкости». Этим замечательным свойством обладают не все растения.
Тяжелые металлы относятся к приоритетным загрязняющим веществам, контроль за содержанием которых является обязательным для объектов окружающей среды (вода, воздух, почва, отходы), промышленной продукции, пищевых продуктов и сырья.
Заведующая санитарно-гигиенической лабораторией филиала Центра гигиены и эпидемиологии в Республике Марий Эл в Советском районе
Источник