- Раствор для ингалятора
- Содержание:
- Классификация препаратов для ингаляций
- Какие растворы подходят для детей
- Какие растворы подходят для взрослых
- Подбор раствора для ингаляции в зависимости от диагноза
- Бронхит
- Бронхоспазм
- Насморк
- Гайморит
- Фарингит
- Ларингит
- Ангина
- Ингаляции сухих порошков – наиболее эффективный способ доставки лекарственных средств в терапии бронхообструктивных заболеваний легких
Раствор для ингалятора
| Статья подготовлена Беликовой Екатериной Вячеславовной, врач, с высшим образованием. Специально для сайта medprostor.by |
Содержание:
При заболеваниях респираторного тракта терапевты часто назначают раствор для ингаляции. Для этого необходимо иметь специальный прибор – небулайзер. Такой способ лечения применим при патологии любого отдела респираторного тракта. Необходимо правильно подобрать раствор и его дозировку, чтобы получить лечебные действия без побочных эффектов.
Классификация препаратов для ингаляций
Выделяется обширная классификация растворов, применяемых для ингаляций. Разновидность препарата зависит от диагноза.
Бронхолитики. Применяются для расширения бронхов при их сужении (обструктивный бронхит, бронхиальная астма). Используя Беродуал, Атровент, Беротек.
Муколитики. Разжижают и выводят мокроту вверх по респираторному тракту. Используются в случае, если мокрота становится слишком вязкой. Применяют Амброксол, АЦЦ, Лазолван.
Противовоспалительные и гормональные средства. Применяют при ларингите и других заболеваниях, сопровождающихся воспалением. Использовать Пульмикорт, Декасан.
Антибактериальные препараты, антисептики. Используют только при доказанной природе инфекционного заболевания, например, трахеит или бронхит с гнойной мокротой. Применяют Фурацилин, Флуимуцил-Антибиотик ИТ.
Антигистаминные средства. Применяют во время аллергии: Кромгексал.
Иммуномодуляторы. Используют в качестве дополнительной терапии, когда человек часто болеет респираторными вирусными инфекциями. Используют Интерферон, Деринат.
Категорически не рекомендуется применение средства самостоятельно. Могут возникнуть серьезные побочные эффекты. Например, если использовать антибиотики при вирусных заболеваниях, состояние пациента может обостриться грибковой инфекцией.
Какие растворы подходят для детей

Раствор для ингаляций включает инструкцию по применению, ей следует строго руководствоваться. На всех средствах указан возраст, с которого можно начинать использовать раствор.
Большинство антибактериальных препаратов для ингаляции применимы только с 2-3 летнего возраста. Гормональные средства рекомендуется применять с 4-6 летнего возраста. Для усиления выведения мокроты при продуктивном кашле используют Амбробене, Амброксол. Они применимы с 3 месяцев. Более серьезным считается Флуимуцил. Его используют с 2 лет.
Чтобы снизить концентрацию препарата, его необходимо развести. Педиатр расскажет, как разводить препарат физраствором для ингаляций, чтобы получить эффект.
Какие растворы подходят для взрослых

Для назначения лекарства учитывают состояние здоровья. Например, если человек страдает от иммунодефицита, не рекомендуется применять ингаляции с антибиотиками. Это вызовет грибковую инфекцию. Гормональные ингаляции не делают людям эндокринными нарушениями.
Если здоровье пациента удовлетворительно, он может использовать любые препараты для ингаляции, в соотношении с определяемыми симптомами болезни. У терапевта узнают, какие растворы для ингаляций применимы.
Подбор раствора для ингаляции в зависимости от диагноза
Лекарственные средства определяются врачом терапевтом, инфекционистом, пульмонологом и другими специалистами в зависимости от поставленного диагноза. Если самостоятельно выбрать раствор, высок риск осложнений, так как нужно знать, как развести раствор для ингаляции правильно.
Многие препараты разбавляют физраствором. Некоторые пациенты не знают, каким физраствором делать ингаляцию. Для этого применяется стерильная жидкость из аптеки, которую набирают шприцем и перемещают в небулайзер.
Не рекомендуется самостоятельно делать физраствор из поваренной соли, так как он должен быть стерилен. Поэтому пациенту нет необходимости знать, как приготовить раствор для ингаляций, его только покупают.
Бронхит
Бронхит – воспалительное заболевания бронхиального дерева. При нем возможен сухой или влажный кашель.
Пертуссин. Разжижает и выводит мокроту. Препарат примененим для влажного и сухого кашля. Обладает сильным противокашлевым действием. Взрослые осуществляют ингаляции до еды по 15 мл 3 раза в сутки. Для детей от 3 до 6 лет используется 5 мл 2 раза в сутки. После 6 лет применяют 10 мл 3 раза в сутки.
Лазолван, Амброгексал. Раствор для ингаляций, разжижающий и выводящий мокроту. В основе средства лежит амброксола гидрохлорид. По инструкции к применению средство используют с 2-летнего возраста в концентрации 2 мл до 2 раз в сутки. Детям старше 6 лет: 3 мл 2 раза в день. Взрослым: 4 мл 3 раза в сутки.
Минеральная вода Боржоми или Нарзан. В них содержится на соль, которая способствует увлажнению слизистой оболочки. Раствор можно применять для любых возрастов. В детском возрасте используют 3-4 мл 2-3 раза в сутки. Взрослым: 5 мл 3-4 раза в сутки.
Хлорофиллипт. Обладает антисептическим эффектом. Подходит для бронхита с гнойной мокротой. Разведение осуществляют в концентрации 1 мл препарата на 10 мл физраствора. Детям делают ингаляции 2 в день по 3 мл раствора. Взрослым можно делать 4 ингаляции в день концентрации 5 мл раствора.
АЦЦ, Флуимуцил. Сильно разжижают и выводят мокроту. Детям с 2 до 6 лет применяют 2 мл средства до 2 раз в день. С 6 до 12 лет дозировка увеличивают до 2 мл 3 раза в сутки. Взрослым можно использовать 3 мм до 4 раз в сутки.
Пульмикорт. Относится к гормональным веществам на основе будесонида. Показан при воспалительном бронхите. Его разводят в соотношении 1 мл препарата на 2 мл физраствора. Детям от 6 месяцев и старше применяют дозировку 0,25- 0,5 мг за 1 сутки. Для взрослых дозировку увеличивают до 2 мг в сутки.

Чтобы не переразжижить мокроту, все дозировки следует соблюдать полностью.
Бронхоспазм
При бронхоспазме сужается просвет бронхов, поэтому мокрота не может выйти наружу.
Беродуал. Расширяет просвет бронхов, степень действия зависит от количества препарата. Для детей до 6 лет средство должно применяться не более 10 капель. Детям старше 6 лет применяют до 40 капель, в зависимости от тяжести заболевания. Взрослым можно применять по 80 капель в тех же критериях.
Пульмовент. Раствор для ингаляций, по инструкции устраняет спазм бронхов. Детям до 6 лет назначают до 12 капель. После 6 лет используют до 24 капель. Взрослым – до 48 капель. Применяют 3-4 раза в день.
Бронхоспазм – опасное состояние, которое необходимо быстрее устранить.

Насморк
Перед проведением ингаляции рекомендуется прочистить носовые ходы, чтобы пары проходили беспрепятственно.
Синупрет. Растительное средство, снимающее воспаление, отек. Обладает небольшим антибактериальным действием. Устраняет воспаление в носовых пазухах. Используют для детей от 2 лет. Его разводят соотношении 1 мл препарата на 2 мл физраствора. Применяют 2 раза в сутки. Для детей от 6 лет разведение 1:2, применяют 2 раза в сутки. Для взрослых разведение 1:1, применяется в 3 раз в сутки.
Эвкалиптовое масло. Препарат разводят в соотношении 7 капель на 100 гр. раствора. Вдхание может осуществляться только с помощью паровых приборов, но не небулайзеров. Обладает увлажняющим, антибактериальным действием. Снимает раздражение и воспаление.
Физраствор. Это наиболее подходящее средство, практически не имеет противопоказаний, применяется в любом возрасте. Родители должны знать, как делать ингаляции с физраствором ребенку. Используют концентрацию 2 мл для детей, 4-5 мл – для взрослых. Ингаляции делают 2-3 раза в сутки. Как заправить ингалятор физраствором: жидкость помещается в контейнер и плотно закручивается крышкой, подсоединяются трубочки и маска.
Также можно применять ингаляции с помощью Нарзана и Боржоми в той же концентрации.

Гайморит
Гайморит – воспалительный процесс в носовых пазухах. Применяются те же препараты, что и при насморке, но обязательно должны употребляться системные антибактериальные средства.
Фарингит
Фарингит – воспаление горла и окружающей лимфоидной ткани.
Тонзилгон Н. Растительное, антисептическое средство. Подходит для детей с самого рождения. Для детей с 1 года применяют 1мл препарата на 2 мл физраствора. Для взрослых используется в отношении 1:1. Используют 1-2 раза в сутки.
Ротокан. Это средство на основе ромашки, календулы. Обладает антисептическим, успокаивающим действием. Для получения необходимой жидкости 10 мл препарата разводят 50 мл физраствора. Для детей используют концентрацию 2 мл 2 раза в сутки, взрослым можно использовать 4мл 4 раз в сутки.
При фарингите средства используются редко, в основном применимы для полоскания.

Ларингит
Ларингит – воспаление гортани, которое сопровождает простудное заболевание.
Дексаметазон. Гормональное средство, показано для снятия воспаления. Как сделать раствор для ингаляции: 2 мл препарата на 2 мл физраствора. Показан к применению с трёхлетнего возраста. Рекомендуется единократное использование для устранения лающего кашля.
Применяют те же препараты, что и при фарингите.
Рекомендовано перед применением гормонального средства проконсультироваться с терапевтом для снижения риска побочных эффектов.

Ангина
Ангина – гнойное воспаление миндалин.
Хлорофиллипт в том же разведении, что и для бронхита.
Мирамистин. Обладает антисептическим, успокаивающим действием. Как приготовить раствор для ингаляции: 2 мл средства на 2 мл физраствора. Ингаляции 2 раза в сутки.

Если появилось побочное действие от выбранного препарата, следует незамедлительно прекратить его употребление. После завершения лечения рекомендуется повторно пройти обследование у врача.
Источник
Ингаляции сухих порошков – наиболее эффективный способ доставки лекарственных средств в терапии бронхообструктивных заболеваний легких
*Импакт фактор за 2018 г. по данным РИНЦ
Читайте в новом номере
Н аучно–технический прогресс привел к совершенствованию различных приспособлений для доставки лекарственных средств (ЛС) в легкие, увеличился арсенал препаратов и нозологические формы заболеваний, где успешно используется ингаляционный путь (ИП) их введения. К примеру, бронхолитические и противовоспалительные средства являются ЛС первой линии для лечения астмы; ацетилцистеин, гипертонические растворы NaCl и антисинегнойные антибиотики – для лечения муковисцидоза; небулизированные растворы адреналина и ГКС – для лечения крупа. Более того, ИП (т.е. местный путь) введения препаратов используется как ворота для доставки ЛС и для системной лекарственной терапии, как в случае применения вакцины против ветряной оспы, противовирусного препарата занамивира для лечения гриппа и инсулина – для лечения диабета и др.
Основные преимущества ингаляционной терапии (ИТ)
Главным преимуществом ИТ является возможность достижения высокой местной и низкой системной концентрации, что и определяет высокий терапевтический индекс (отношение желаемых и нежелательных эффектов) ЛС и возможность их доставки непосредственно к органам–мишеням и рецепторам, от чего зависит быстрота наступления положительного эффекта и безопасность. При этом нежелательные эффекты не являются значимыми, так как в результате эффекта первого прохождения через печень в системный кровоток поступает только незначительная часть неизмененного препарата в случае применения иГКС (терапевтический индекс флютиказона пропионата, беклометазона дипропионата и будесонида составляет ≤1 в отличие от гидрокортизона) [1]. Для профилактики местного кандидоза можно варьировать выбором ГКС, типом ингалятора и полосканием ротовой полости после ингаляции. При применении бронхолитиков следует ориентироваться на такие свойства b 2 –агонистов, как селективность, сродство к b 2 –рецептору (полный или частичный агонист), быстроту наступления и длительность бронхолитического эффекта и т.д.
Чем должен руководствоваться врач
при назначении ИТ?
Приспособления или средства для доставки ЛС в легкие (ингаляторы) должны отвечать следующим потребностям: для больных – наиболее значимыми факторами являются размеры ингаляторов, простота в использовании, раздражаемость, вкус, запах и другие свойства (например, стоимость), которые окажут влияние на комплаентность и в целом на эффективность; врач должен знать особенности строения бронхиального дерева (БД), аэродинамические свойства воздушного потока, где в перемешанном с воздухом виде содержатся частицы ЛС, о количествах препарата, достигающих определенных участков в легких при использовании разнообразных типов ингаляторов больными, в зависимости от возраста и клинического статуса; для регуляторных органов важно иметь in vitro результаты по воспроизводимости точного определения количества доставляемого препарата. Например, если для b 2 –агонистов можно допустить легкую погрешность в точности из–за «широты» терапевтического индекса препаратов, то для ГКС и инсулина, препаратов с «узким» терапевтическим индексом, точность в воспроизводимости количества доставляемого ЛС обязательна.
В настоящее время врач довольно легко принимает решение начать терапию астмы и ХОБЛ ингаляциями b 2 –агонистов, иГКС в соответствии с рекомендациями международных или национальных руководств, так как их эффективность и безопасность доказана с высоким уровнем доказательности (уровень А) [2,3]. Причем ингаляция сухих порошков является самым надежным и эффективным способом ИТ, что делает их средствами первой линии для терапии больных астмой и ХОБЛ, особенно на этапе поддерживающей терапии в условиях амбулаторной помощи.
Однако на практике врач испытывает значительные трудности в выборе групп и путей введения препаратов, равно как и в выборе типов ингаляторов, а также в простом и доступном разъяснении основных правил пользования тем или иным ингалятором, так как точное следование больными этим указаниям отражается на комплаентности и, в конечном счете, на эффективности терапии.
Анатомические
и функциональные особенности строения бронхиального дерева
Для ингаляции сухих порошков требуется: а) приспособление для доставки ЛС в легкие, которое определяет аэродинамические и механические свойства воздушного потока; б) фармацевтический продукт с его специфическими, присущими ЛС, физико–химическими свойствами.
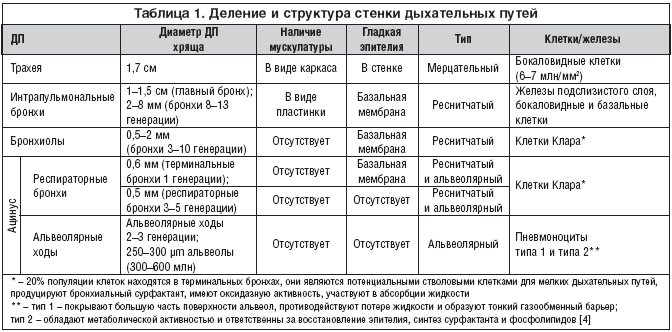
Несмотря на кажущуюся простоту проведения ИТ, нужно учесть, что ингалируемый препарат в составе воздушного потока проходит очень сложный путь до места их отложения и проявления фармакологической активности, так как само строение бронхиального дерева и функциональные особенности очень различаются в направлении от центра к периферии (табл. 1).
Как видно из таблицы 1, по направлению к периферии не только уменьшается калибр дыхательных путей (ДП), но меняется и структура строения их стенки, исчезает гладкая мускулатура в зоне ацинуса, включающего респираторные бронхи 3–5 генерации и альвеолярные ходы, т.е. калибр и состояние последних не будут подвергаться влиянию дыхательного цикла. В этих областях отсутствуют слизистые железы, происходит активная абсорбция жидкости (соответственно и ЛС), продуцируется сурфактант, препятствующий спадению альвеол. При вдохе воздушный поток развивает большую скорость, встречая на своем пути преграду в виде бифуркации трахеи, движение потока замедляется и меняется его характер. Он становится турбулентным, а на самой периферии, в респираторных бронхиолах (ацинусе), где отсутствует гладкая мышца, молекулы газа в воздухе остаются во взвешенном состоянии и, сталкиваясь между собой, приобретают хаотичный характер. Таким образом, в процессе дыхания меняется характер движения воздушного потока: с ламинарного в трахее, он становится турбулентным (завихренным) в проксимальных и в терминальных отделах, а далее в респираторных бронхиолах (в ацинусе) – хаотичным (броуновское движение).
Вдыхаемые же частицы ЛС, подвергаясь действию механических и электрических сил, меняют траекторию своего движения, которая несколько отличается от линии воздушного потока. Они движутся к поверхности ДП, причем если все вдыхаемые частицы подвергаются действию механических сил, то только заряженные частицы – действию электрических сил.
Поэтому транспорт частиц ЛС в ДП, перемешанных с воздухом, происходит их механическим перемещением – инерционным, диффузионным и гравитационным и зависит от калибра путей.
Инерционный транспорт (инерционное перемещение, столкновение частиц).Вдыхаемый воздух меняет вязкость и направление движения по мере поступления в легкие. Для частичек с массой более 6 µm в диаметре вышеуказанные силы приводят к инерционному перемещению, которое нарастает с увеличением вязкости, диаметра и плотности частиц, поэтому инерционное отложение частиц будет наибольшим в зоне с максимальной вязкостью воздушного потока, т.е. в крупных ДП.
Диффузионный транспорт частиц (диффузионное перемещение). Величина вдыхаемых частиц ЛС сопоставима с молекулами газа (около 0,6 µm). При каждом их столкновении с молекулой газа в ДП изменяется кинетическая энергия и направление движения частичек. Их движение становится хаотичным и беспорядочным (броуновское движение или диффузия). Максимальное отложение их происходит на периферии, в ацинусе, в области, где время задержки частиц максимальное.
Гравитационный транспорт (гравитационное перемещение или осаждение частиц). Частички размером более 0,1 µm (до 3 µm) в диаметре больше подвергаются процессу гравитации, чем диффузии. Гравитационное перемещением увеличивается со временем, с увеличением размера и плотности частиц, большее их отложение происходит также на периферии и в зоне ацинуса.
ИТ и клетки–мишени
Понятно, что одним из условий оптимизации эффективности действия ингалируемых ЛС является доставка адекватной дозы препарата как можно ближе в те зоны, в которых располагаются клетки–мишени и/или рецепторы, гладкая мускулатура, «воспалительные» клетки, различающиеся у противоастматических групп ЛС.
Бронхолитики. b 2 –агонисты короткого и длительного действия (сальбутамол, тербуталин, фенотерол, сальметерол, формотерол) расслабляют гладкую мускулатуру бронхов посредством стимуляции b 2 –адренорецепторов ( b 2 –АР), в то время как М–холиноблокаторы (М–ХБ) короткого и длительного действия (ипратропиум – и тиотропиум бромид) предупреждают сокращение гладкой мускулатуры посредством блокады М–холинорецепторов (М–ХР).
Локализация b 2 –АР и М–ХР. С помощью ауторадиографических исследований с использованием световой микроскопии P. Barnes с соавторами показали, что b –АР располагаются вблизи гладкой мускулатуры бронхов с увеличением их количества в мелких бронхах [5]. Они были найдены в большом количестве и в альвеолах. Этим фактом, по–видимому, можно обосновать эффективность небулайзерной терапии сальбутамолом (системная доставка сальбутамола) при острой тяжелой бронхообструкции.
Плотность М–ХР, в том числе и более специфичных М3–ХР, в легких очень высокая, преимущественно они располагаются в крупных ДП и меньше – в периферических. В большом количестве М3–ХР найдены и в железах подслизистого слоя.
Гладкая мускулатура. У здоровых лиц количество гладкой мускулатуры уменьшается в направлении от крупных ДП к периферии, в то время как у больных астмой на аутопсии было выявлено его увеличение во всех бронхах, а снижение к периферии было менее значимым. Кроме того, при наличии астмы были выявлены 2 типа их увеличения в бронхах: тип 1 – с их увеличением только в крупных ДП и тип 2 – с увеличением их и в крупных, и в мелких бронхах [6].
Противовоспалительные ЛС. При ИТ ГКС, динатрия кромогликатом, недокромилом натрия больных астмой основной клеткой–мишенью являются эозинофилы [2]. ГКС снижают количество циркулирующих эозинофилов и их накопление в легких, уменьшают их выживаемость и продукцию цитокинов, ответственных за привлечение эозинофилов в эти процессы. Кромоны тормозят способность эозинофилов вызывать экспрессию клеток воспаления (комплемента С3b и Fc γ –рецепторы). Недокромил ингибирует высвобождение белков из эозинофильных гранул и образование лейкотриенов (LTC4) эозинофилами.
Распределение эозинофилов. У больных астмой количество эозинофилов в ДП увеличено. На аутопсии, у умерших больных астмой, они также были увеличены. Причем без различий по тяжести астмы и длительности срока от начала тяжелого обострения – в течение 1 часа от начала приступа или на фоне тяжелых приступов, длящихся от нескольких часов до нескольких дней, больных с фатальной астмой по сравнению с умершими без астмы (контрольная группа). Обнаружено увеличение в проксимальных отделах бронхов эозинофилов – 62,7 против 1,0; активированных эозинофилов 35,7 против 0. Также были увеличены Т–лимфоциты – 72,8 против 27,9; лейкоциты – 96,9 против 41 соответственно. Таким образом, выявлена преимущественная клеточная инфильтрация, особенно эозинофилами, проксимальных отделов, что предполагает центральную локализацию воспалительного процесса [7].
ГКС – рецепторы (ГКС–Р). В легких ГКС–Р распространены повсеместно, хотя наибольшая их плотность обнаружена в стенках альвеол, на эндотелии сосудов, на клетках гладкой мускулатуры бронхиальных и легочных сосудов, причем без различий как у больных астмой, так и с отсутствием астмы у лиц в контрольной группе [8]. Небольшое количество ГКС–Р локализуется в эпителии ДП и гладкой мышце, также без разницы у больных астмой или с ее отсутствием.
Тучные клетки (ТК). Кромогликат и недокромил натрия ингибируют не только различные звенья экспрессии эозинофилов и секрецию цитокинов, но благодаря их способности стабилизировать мембраны ТК, они предотвращают их дегрануляцию и, следовательно, высвобождение медиаторов воспаления. В настоящее время открыты 2 типа ТК, отличающихся по секреторной активности: ТКтс–клетки содержат химазу, карбоксипептидазу, катепсин– G–подобную протеазу и триптазу. Эти клетки располагаются преимущественно на коже и в слизистой ЖКТ; ТМт–клетки содержат только одну триптазу, они локализуются преимущественно в альвеолах [9].
Таким образом, частицы ЛС должны доставляться в зоны наибольшей плотности клеток–мишеней (гладкая мускулатура, эозинофилы) и рецепторов, т.е. к крупным и мелким бронхам, что вполне обеспечивается ингаляциями сухих порошков при стабильном состоянии и в период обострения астмы, так как воспалительный процесс преимущественно локализуется в проксимальных отделах.
Факторы, влияющие
на эффективность ИТ
сухими порошками
Типы порошковых ингаляторов (ПИ). Первым успешным ПИ для однодозовой ингаляции динатрия кромогликата был спинхалер (Fisons). В последующем появились ингаляторы с различным принципом дозирования: ротахалер (GlaxoSmithKline, UK) и циклохалер/айролайзер (ISF, Italy; Novartis, Switzeland), хандихалер и др. для однодозовой ингаляции капсулы. Дискхалер (GlaxoSmithKline, UK), который уже является многодозовым ингалятором, с применением диска, содержащего 4 или 8 доз, Дискус/Аккухалер (GlaxoSmithKline, UK) появился в середине 90–х гг. XX века, где использована та же система диска с полосками блистера из фольги, в котором заключена каждая из 60 доз препарата.
Турбухалер. Современный ингалятор Турбухалер (AstraZeneca, Sweden) является мультидозовым резервуарного типа ингалятором, содержащим многократные дозы, с дозирующим устройством для гарантированного измерения каждой дозы, независимо от количества препарата, остающегося в резервуаре. Заряжается ингалятор (т.е. замер одной дозы) простым поворотом зарядного устройства (нижняя часть ингалятора) сначала до упора в одну, затем в другую сторону – и ингалятор готов для использования. При вдыхании воздух проходит через участок дозирующего диска с отверстиями, где потоком захватывается отмеренная доза порошка и поступает в ингаляционный канал, затем в зону дезагрегации – к двум спиральным каналам в мундштуке, где аэродинамические свойства создают турбулентный поток воздуха (почему ингалятор и получил название «Турбухалер»). При интенсивном перемешивании порошка и воздуха происходит диспергизация порошка с образование мельчайших частичек ЛС диаметром
Внутреннее сопротивление ингалятора, присущее всем ПИ, отличается у разных ПИ [12]. Чем оно выше, тем может быть ниже респираторный поток для эффективного отложения препарата в легких и потребуется меньше усилий для вдыхания. Это означает, что работа ПИ с низким сопротивлением более чувствительна к степени бронхообструкции больного, чем ПИ с высоким внутренним сопротивлением. Например, для Турбухалера, ПИ с присущим высоким внутренним сопротивлением, равном 0,100 см водного столба/л/мин., потребуется меньший инспираторный поток (около 30 л/мин.), в то время как для Ротахалера с внутренним сопротивлением 0,040 см водного столба/л/мин инспираторный поток должен составлять около 70 л/мин. Таким образом, больной с выраженной обструкцией бронхов способен эффективно пользоваться ПИ Турбухалером, но не ротахалером, и в этом – несомненное преимущество Турбухалера.
Успех ИТ в большинстве случаев зависит от способности больного вызвать адекватный инспираторный поток, зависящие от возраста, ментальности и состояния больного. При глубоком медленном вдохе увеличивается отложение препаратов в периферических ДП, в то время как глубокий и быстрый вдох вызывает увеличение инерционного отложения частиц в верхних ДП и крупных бронхах и меньше – в периферические ДП. Частое и поверхностное дыхание увеличивает потерю препарата из–за увеличения мертвого пространства.
Все существующие на сегодняшний день ингаляторы для вдыхания сухих порошков – ПИ управляются усилием вдоха больных для того, чтобы лекарство (смесь лактозы с микроионизированным препаратом) покинуло резервуар, дозирующий диск, блистер, капсулу и т.д. При этом различия в аэродинамических и механических свойствах ингаляторов оказывает большое влияние на легочное отложение частиц препарата и эффект терапии, а потому каждая комбинация ингалятор + фармацевтический продукт разрабатывается компанией только для собственного продукта.
Нельзя использовать, например, капсулу для ингалятора Айэролайзер в Ротахалере или наоборот. Поэтому понятно существование большого количества разнообразных типов ПИ, хотя принцип их действия приблизительно одинаков.
Для ПИ наиболее оптимальный уровень инспираторного потока колеблется в пределах 30–120 л/мин. Для Турбухалера он наименьший – от 30 до 60 л/мин., что делает его применимым у детей и даже при тяжелой бронхообструкции, например, при обострениях астмы, когда в большей степени снижается экспираторный поток (ОФВ 1 ), а инспираторный поток составлял в среднем 60 л/мин., с колебаниями от 30 до 90 л/мин. [13].
Обычно легочное отложение препарата из ПИ уступает таковому из дозированных аэрозольных ингаляторов (ДАИ). Это было показано в исследованиях с радиоизотопной меткой сальбутамола, ингалируемого из ПИ и ДАИ здоровыми добровольцами, где % отложения от номинальной дозы составлял 12,5% (ПИ) и 22% (ДАИ) и несколько меньше у больных астмой – 11,4% (ПИ) и 18,2% (ДАИ) соответственно [10]. В то же время альвеолярное отложение будесонида, определенное измерением системной биодоступности у здоровых добровольцев при ингаляции из ПИ Турбухалер, вдвое превышало этот показатель при ингаляции из ДАИ – 32% против 15% [11].
Эти данные могут свидетельствовать о том, что частички ЛС из Турбухалера в значительной мере подвергаются диффузионному перемещению в периферические отделы ДП, где происходит интенсивное их всасывание с высокой системной биодоступностью препарата. Подтверждением этого факта могут служить данные о быстроте наступления положительного эффекта будесонида (Пульмикорта суспензии) при его применении через небулайзер у больных при острой тяжелой астме по сравнению с назначением системных ГКС [14].
Размеры частиц. На эффективность ИТ ПИ оказывают влияние размеры частиц, частота дыхания и объем дыхания. Для частиц размером >3 µm механическое столкновение при высокой скорости может привести к потере ЛС в ротоглотке и трахее и увеличенное их отложение в проксимальных ДП, в трахее и в крупных бронхах. Поэтому медленный и глубокий вдох увеличивает отложение этих частиц на периферии. Для частиц, которые откладываются механическим осаждением, с размерами частиц >0,5
Было показано, что инспирабельная доза, определяемая как доза препарата с частичками
Поэтому при производстве порошков, они должны измельчаться для получения необходимых размеров, однако при их использовании в ингаляторе может возникнуть проблема с адгезией, связанной с Ван дер Ваальсовой и электростатической силами, и повторным образованием частиц больших размеров, которые будут осаждаться в крупных ДП. Проблема решается использованием вспомогательных веществ – лактозы или глюкозы, в качестве переносчика микроионизированного препарата, предохраняющих последний от аггломерации. Успешно применяется лактоза в перемешанном виде с микроионизированным лекарством, например, для Оксиса (формотерол и лактоза) и Симбикорта (будесонид, формотерол и лактоза) Турбухалер. В ДП путях ингалированный препарат освобождается от лактозы, в виде кристаллов откладывается на слизистой ДП и в дальнейшем подвергается диффузионному или гравитационному перемещению в ее слизистой. Для предотвращения адгезии поверхности лактозы придают шаровидную или неправильную с выступами формы. Было показано, что шаровидная форма лактозы способна перенести на себе большее количество инспирабельных частиц ЛС, особенно это касается применения больших доз препаратов. Например, в Дискусе с содержанием 500 мкг флютиказона переносится 120 мкг препарата, что составляет примерно 24% от номинальной дозы, в виде инспирабельных частиц по сравнению 7 мкг (14% от номинальной дозы) в случае применения дозы 50 мкг флютиказона Дискус. Другой путь решения проблемы с адгезией состоит в превращении в большие сфероидные образования мельчайших частичек самих лекарств диаметром 2–4 мкм в фармацевтическом продукте, т.е. применяется чистое лекарство без переносчика, как сделано в случае Пульмикорта (будесонид) Турбухалер.
Отложение частиц в легких. Следует отметить, что отложение частиц в легких отличается у разных ПИ, при этом наблюдаются весьма значимые колебания, в пределах 5–30% от измеренной дозы. Поэтому результаты, полученные при исследовании одного ПИ, нельзя экстраполировать на другой ПИ. Для дискхалера, дискуса и ротахалера, где использован аналогичный фармацевтический принцип, легочное отложение ЛС небольшое и составляет 10–12% (дискхалер и дискус), еще меньше – 5% у ротахалера [16]. Легочное отложение для Турбухалера колеблется от 16,8 до 20–30% и более (25–40%) на обычном для ингалятора инспираторном потоке – около 60 л/мин. (30–60 л/мин.) как у взрослых добровольцев, так и у больных астмой [17,18]. При сравнении двух наиболее употребляемых ПИ Турбухалера и Дискуса были выявлены различия не только в количестве легочного отложения, но еще в большей степени в его вариабельности (как у детей, так и у взрослых). При сравнении легочного отложения и его вариабельности при ингаляции будесонида из Турбухалера и флютиказона через Дискус у детей был показан больший процент отложения будесонида при ингаляции из Турбухалерла – 30,8% по сравнению с 8% при ингаляции флютиказона из Дискуса, а вариабельность из Турбухалера составила 24,3% против 61,2% из Дискуса [19]. Подобные результаты были получены и у взрослых: у добровольцев легочное отложение будесонида и его вариабельность при ингаляции из Турбухалера составляли 36 и 21%, и у больных астмой – 38 и 9% соответственно, в то время как эти же показатели при ингаляции флютиказона через Дискус составили соответственно 13 и 40% у добровольцев и 14 и 37% у больных астмой [20].
Как указывалось выше, имеется прямая зависимость между отложением частиц инспирабельной дозы от их размера и глубины инспираторного потока. У больных и у здоровых отложение частиц с диаметром 1–3 µm может также колебаться в зависимости от задержки дыхания, отношения ОФВ 1 /ЖЕЛ, вдоха, величины остаточного объема. Отложение частиц различалось при диаметре 1–2 µm и отсутствовало при диаметре 3 µm (при скорости потока = 250 мл/с без задержки дыхания). Причем отложение частиц с диаметром 1 µm было обратно пропорционально отношению ОФВ 1 /ЖЕЛ, вдоху и величине МЕF 50. Эти корреляции отсутствовали при больших диаметрах частиц. При повторном исследовании уже с задержкой дыхания на 6 сек исчезали различия в отложении частиц с диаметром 1 и 2 µm, возможно, из–за увеличения времени соприкосновения частиц [21].
Эти данные, по–видимому, являются обоснованием для рекомендации глубокого вдоха, длительностью 6 сек, при спирометрических исследованиях у больных астмой.
У здоровых и больных с различной степенью бронхообструкции сравнивали отложение частиц ингалированных аэрозолей диаметром 1,2 µm с радиометкой ТС с определением индекса пенетрации частиц в легкие, при этом допускали, что высокий индекс означает большее отложение. Было найдено, что этот индекс высоко коррелировал с ОФВ 1 должной величины (r=0,91, p
Комплаентность. Как указывалось выше, ошибки в технике ингаляции снижают доставляемую дозу к рецепторам и клеткам–мишеням, и это может изменить эффективность терапии. Поэтому для успеха терапии очень важно, чтобы больной понимал сущность принимаемой терапии, умел правильно пользоваться ПИ и следовал предписанию врача.
Так, комплаентность, оцененная при помощи самоконтроля и измерения веса контейнеров с ЛС (т.е. ингаляторов) в LHS, изучалась в двухлетнем клиническом исследовании ипратропиума бромида у больных ХОБЛ, и было выявлено, что только 70% больных следовали предписанию врача [24]. В других клинических исследованиях, проведенных с использованием системы электронного мониторинга, было показано, что 40% больных «недопринимали» ЛС, а 20% – принимали больше предписанного, причем ретроспективные данные из Новой Зеландии показывают, что для иГКС ежедневная доза из ПИ была выше, чем доза из ДАИ [25].
О необходимости постоянного обучения технике ингаляции и контроля по использованию ингаляторов больными свидетельствуют данные о том, что 88% больных астмой и ХОБЛ, использовавшие ДАИ или ПИ, демонстрировали, по крайней мере, 1 ошибку. Через 2 недели после инструктирования у больных снова возникали проблемы по применению, поэтому обучение и контроль необходимо повторять периодически. Было показано, что пациенты, неспособные управлять одним типом ингаляторов, при переводе на другой тип, успешно справлялись с ними. Поэтому нужно выработать тактику для рациональной стратегии, беря во внимание различные факторы, такие как возраст, способность обучаться правильному использованию и принимать во внимание предпочтение больных [26].
Комплаентность может быть улучшена не только регулярным инструктированием и образованием больных, но и путем снижения частоты приема дневной дозы или использования одного ингалятора для поддерживающей и спасательной терапии, как, например, при применении комбинированного препарата Симбикорт Турбухалер в режиме SMART у больных бронхиальной астмой.
На современном этапе ингаляции сухих порошков – бронхолитиков, стероидных и нестероидных противовоспалительных препаратов, являются средствами первой линии для поддерживающей терапии больных астмой и ХОБЛ в амбулаторных условиях. Для успешного лечения и оптимизации эффективности терапии врач должен осознанно выбирать тип ингалятора с учетом анатомического и функционального строения бронхиального дерева, аэродинамических свойств ингалятора, количества и вариабельности доставляемого препарата к клеткам–мишеням и рецепторам в зависимости от клинического состояния и способности больного создать оптимальный инспираторный поток. Турбухалер может иметь преимущество, легочное отложение частиц ЛС из которого составляет 20–40% от номинальной дозы и сопровождается меньшими колебаниями в количестве доставляемого препарата. Ингаляции осуществляются при низких значениях инспираторного потока, который может генерировать и взрослый больной с различной степенью бронхообструкции, и дети. Необходимо обучать больных технике ингаляции и осуществлять контроль за использованием ингаляторов.
Литература
1. Phillips JE, Natielli M, Kelly G et al. Allergic rat ashma model to asses the therapeutic index of inhaled corticoseroids. AJRCCM 2008; Abstracts issue: v 177: A 218
2, Global initiative for asthma. Global strategy for asthma management and prevention. Workshop report,2007. /www.ginasthma.com/
3. Global initiative for chronic obstructive lung disease (GOLD). Global strategy for diagnosis, management and prevention of chronic obstructive pulmonary disease. NHBI/WHO workshop report. Last updated 2007/ www.gold.org/.
4.Grapo JD et al. Cell characteristics of the normal lung. Am Rev Respir Dis 1982; 125: 740–745
5. Barnes PJ et al. Autoradiographic localization of autonomic receptors in airway smooth muscle.Am Rev Respir Dis 1983; 127: 758–762
6. Ebina S, Yaegashi H et al. Hyperactive site in the airways tree of asthmatic patirntss revealed by thickening of bronchial musclrs. Am Rev Respir Dis 1990; 141: 1327–1332
7. Faul JL, Tormey VJ, Leonard C et al. Lung immunopathology in cases of sadden death. Eur Respir J 1997; 10: 301–307
8. Adcock IM, Gilbey T et al. Glucocorticoid receptor locazation in normal and asthmatic lung. AJRCCM 1996; 154: 771–782
9. Schwartz L, Huff T. Biology of mast cells and basophils. In: Middleton E Jr et , es. Allergy principles and practice. v 1 Baltimore: Mosby, 1993: 140–141
10. Newman S et al. Terbutaline sulphate : effect of inhaled flow rate on drug deposition and efficacy. Int J Pharmacol 1991; 74: 209–213
11. Engel T et al. Effects, side effects and plasma concentrations of terbualine in adult asthmatics after inhaling from powder inhaler devise at different flows and volumes. Br J Clini Pharmacol 1992; 33: 439–444
12. Clark AR, Hollingworh AM. The relationship between powder inhaler resistance and peak inspiratory conditions in healthy volunteers–implications for in vitro testing. J Aerosol Med 1993; 6: 99–110
13. Brown P et al. Peak inspitatory flow through Turbuhaler in acute asthma. Eur Respir J 1995; 8: 1940–1941
14. Rodrigo G, Rodrigo S Corticoseroids in the emeency department therapy of acute adult asthma. Chest; 1999: 116, p 285–295
15. Steckel H, Muller BW. In vitro evalution of dry powder inhalers: 1. Drug deposition of commonly used devices. Int Pharm 1997; 154: 19–29
16. Pedersen S et al. Influence of inspiratory flow rate upon the effect of a Turbuhaler. Arch Dis Child 1990; 55: 308–310
17. Thorsson L et al. Lung deposition of budesonide in asthmatics : comparison of different formulation. Int J Pharm 1998; 168: 119–127
18. Selroos O
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Источник